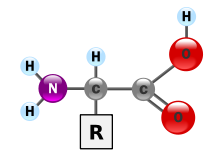
Aminosäuren (AS), unüblich aber genauer auch Aminocarbonsäuren, veraltet Amido<a class=”image” href=”https://de.wikipedia.org/wiki/Datei:AminoAcidball.svg”>säuren genannt, sind chemische Verbindungen mit einer Stickstoff (N) enthaltenden Aminogruppe und einer Kohlenstoff (C) und Sauerstoff (O) enthaltenden Carbonsäuregruppe.1Georg Löffler: Biochemie und Pathobiochemie. Springer-Verlag, 2013, ISBN 978-3-662-06062-9, S. 25. Aminosäuren kommen in allen bekannten Lebewesen vor. Sie sind die Bausteine von Proteinen (Eiweiß) und werden frei bei der Zerlegung von Proteinen (Proteolyse). Essentielle Aminosäuren kann ein Organismus nicht selber herstellen, sie müssen daher mit der Nahrung aufgenommen werden.
Zur Klasse der Aminosäuren zählen organische Verbindungen, die zumindest eine Aminogruppe (–NH2 bzw. substituiert –NR2) und eine Carboxygruppe (–COOH) als funktionelle Gruppen enthalten, also Strukturmerkmale der Amine und der Carbonsäuren aufweisen. Chemisch lassen sie sich nach der Stellung ihrer Aminogruppe zur Carboxylgruppe unterscheiden – steht die Aminogruppe am Cα-Atom unmittelbar benachbart zur endständigen Carboxygruppe, nennt man dies α-ständig und spricht von α-Aminosäuren.
Ausgewählte α-Aminosäuren sind die natürlichen Bausteine von Proteinen. Sie werden miteinander zu Ketten verknüpft, indem die Carboxygruppe der einen Aminosäure mit der Aminogruppe der nächsten eine Peptidbindung eingeht. Die auf diese Weise zu einem Polymer verketteten Aminosäuren unterscheiden sich in ihren Seitenketten und bestimmen zusammen die Form, mit der das Polypeptid im wässrigen Milieu dann zum nativen Protein auffaltet. Diese Biosynthese von Proteinen findet in allen Zellen an den Ribosomen nach Vorgabe genetischer Information statt, die in Form von mRNA vorliegt.
Die Basensequenz der mRNA codiert in Tripletts die Aminosäurensequenz, wobei jeweils ein Basentriplett ein Codon darstellt, das für eine bestimmte proteinogene Aminosäure steht. Die hiermit als Bausteine für die Bildung von Proteinen in einer bestimmten Reihenfolge angegebenen Aminosäuren formen die Proteine.2Katharina Munk (Hrsg.): Biochemie – Zellbiologie. Georg Thieme Verlag, Stuttgart 2008, ISBN 978-3-13-144831-6, S. 122, Google Books. Beim Menschen sind es 21 verschiedene proteinogene Aminosäuren, neben den standardmäßig 20 (kanonischen) Aminosäuren auch Selenocystein. Nach der Translation können die Seitenketten einiger im Protein eingebauter Aminosäuren noch modifiziert werden.
Das Spektrum der Aminosäuren geht allerdings über diese rund zwanzig proteinogenen weit hinaus. So sind bisher über 400 nichtproteinogene natürlich vorkommende Aminosäuren bekannt, die biologische Funktionen haben.3Peter Nuhn: Naturstoffchemie. S. Hirzel Wissenschaftliche Verlagsgesellschaft, Stuttgart 1990, ISBN 3-7776-0473-9, S. 70.Die vergleichsweise seltenen D-Aminosäuren stellen hierbei eine spezielle Gruppe dar.4G. Genchi: An overview on D-amino acids. In: Amino Acids. Band 49, Nummer 9, September 2017, S. 1521–1533, doi:10.1007/s00726-017-2459-5. PMID 28681245. Die Vielfalt der synthetisch erzeugten und die der theoretisch möglichen Aminosäuren ist noch erheblich größer.
Einige Aminosäuren spielen als Neurotransmitter eine besondere Rolle, ebenso verschiedene Abbauprodukte von Aminosäuren; biogene Amine treten nicht nur als Botenstoffe im Nervensystem auf, sondern entfalten auch als Hormone und Gewebsmediatoren vielfältige physiologische Wirkungen im Organismus.
Die einfachste Aminosäure, Glycin, konnte nicht nur auf der Erde, sondern auch auf Kometen, Meteoriten und in Gaswolken im interstellaren Raum nachgewiesen werden.5NASA Researchers Make First Discovery of Life’s Building Block in Comet. nasa.gov, August 2009; Chiral amino acids in meteorites strengthen evidence for extraterrestrial life. spie.org, September 2010 (abgerufen am 4. Oktober 2010).
Inhaltsverzeichnis
- 1 Geschichte
- 2 Struktur
- 3 Aminoacyl-Gruppe
- 4 Proteinogene Aminosäuren
- 5 Nichtproteinogene Aminosäuren
- 6 Nachweis
- 7 Gewinnung und Produktion
- 8 Verwendung
- 9 Metabolismus
- 10 Siehe auch
- 11 Literatur
- 12 Weblinks
Quellen und Tiefen
- 1Georg Löffler: Biochemie und Pathobiochemie. Springer-Verlag, 2013, ISBN 978-3-662-06062-9, S. 25.
- 2Katharina Munk (Hrsg.): Biochemie – Zellbiologie. Georg Thieme Verlag, Stuttgart 2008, ISBN 978-3-13-144831-6, S. 122, Google Books.
- 3Peter Nuhn: Naturstoffchemie. S. Hirzel Wissenschaftliche Verlagsgesellschaft, Stuttgart 1990, ISBN 3-7776-0473-9, S. 70.
- 4G. Genchi: An overview on D-amino acids. In: Amino Acids. Band 49, Nummer 9, September 2017, S. 1521–1533, doi:10.1007/s00726-017-2459-5. PMID 28681245.
- 5NASA Researchers Make First Discovery of Life’s Building Block in Comet. nasa.gov, August 2009; Chiral amino acids in meteorites strengthen evidence for extraterrestrial life. spie.org, September 2010 (abgerufen am 4. Oktober 2010).
Quellen und Tiefen
- 1Georg Löffler: Biochemie und Pathobiochemie. Springer-Verlag, 2013, ISBN 978-3-662-06062-9, S. 25.
- 2Katharina Munk (Hrsg.): Biochemie – Zellbiologie. Georg Thieme Verlag, Stuttgart 2008, ISBN 978-3-13-144831-6, S. 122, Google Books.
- 3Peter Nuhn: Naturstoffchemie. S. Hirzel Wissenschaftliche Verlagsgesellschaft, Stuttgart 1990, ISBN 3-7776-0473-9, S. 70.
- 4G. Genchi: An overview on D-amino acids. In: Amino Acids. Band 49, Nummer 9, September 2017, S. 1521–1533, doi:10.1007/s00726-017-2459-5. PMID 28681245.
- 5NASA Researchers Make First Discovery of Life’s Building Block in Comet. nasa.gov, August 2009; Chiral amino acids in meteorites strengthen evidence for extraterrestrial life. spie.org, September 2010 (abgerufen am 4. Oktober 2010).
Hauptquellen der Texte und Materialien:
Internationale Wikipedias. Wurde evtl. ganz oder teilweise ins Deutsche übersetzt. Unter der Creative Commons Attribution-Share-Alike License 4.0 verfügbar; zusätzliche Bedingungen können gelten. Durch die Nutzung dieser Website erklären Sie sich mit den Nutzungsbedingungen und der Datenschutzrichtlinie einverstanden.
Weitere extensive und evtl. aktuellere Ausführungen finden Sie in den zitierten Wikipedia-Artikeln.